De gevestigde mening is dat de huidskleur van onze voorouders die naar hogere breedtegraden migreerden, licht van kleur moest worden om voldoende vitamine D te kunnen maken voor het behoud van hun calciumbalans. Het verlies van het huidpigment melanine staat daarbij dus centraal. Nieuwe inzichten uit de archeologie en de genetica leren ons echter dat we deze gedachte moeten nuanceren.

Vitamine D is een dinosaurus onder de biomoleculen.1,2-2d Het heeft talrijke functies; niet alleen in het calcium/fosfaatmetabolisme van het bot, maar bijvoorbeeld ook in het neuromusculair systeem (spiercontractie), groei en ontwikkeling (kanker), glucose-homeostase (diabetes), hersenfunctie (depressie), cardiovasculair systeem (hypertensie) en immuunsysteem.3,4 Vitamine D-tekort op jonge leeftijd veroorzaakt rachitis. Dat wordt vooral gekenmerkt door onvoldoende calcificatie van het groeiende bot. Het presenteert zich als afwijkingen van het skelet, zoals kromme benen (O- of X-benen), maar ook een vervorming van het bekken. Door laatstgenoemde is een normale vaginale geboorte niet meer mogelijk, hetgeen een evident evolutionair nadeel is.3a
Eigenlijk is vitamine D geen vitamine. We kunnen vitamine D3 maken uit 7-dehydrocholesterol (7DHC), hetgeen ook de voorloper is van cholesterol. Hiervoor dient 7DHC in onze huid te worden blootgesteld aan de ultraviolette B (280-320 nm) straling van de zon. De optimum synthese ligt bij 280 nm. 7DHC en uvB vormen onze belangrijkste bron van vitamine D3. Met uitzondering van de gehaltes in vis(lever) (vitamine D3) en paddenstoelen (vitamine D2) zijn de gehaltes in onze voedingsproducten laag. Voor zijn werkzaamheid dient vitamine D te worden omgezet naar 25-hydroxyvitamine D (25OHD), dat op zijn beurt kan worden omgezet in 1,25-dihydroxyvitamine D (1,25OHD). Deze omzettingen vinden respectievelijk plaats in de lever en de nieren (voor vitamine D’s endocriene functie), maar waarschijnlijk is iedere cel die vitamine D of 25OHD kan opnemen, in staat het vervolgens om te zetten naar 1,25OHD voor autocriene en paracriene functies (extra-renale synthese)3,4. 1,25(OH)D fungeert als hormoon door binding aan de vitamine D-receptor (VDR). Inzake vitamine D’s functie kan onderscheid worden gemaakt in de calcemische en niet-calcemische functies van vitamine D. Mechanistisch worden onderscheiden de snelle reacties via interactie van 1,25OHD met de membraan en de genomische reacties via interactie met ons genetisch materiaal in de celkern. Ongeveer 3% van ons genoom wordt direct of indirect aangestuurd door vitamine D’s endocriene systeem.4a,4b
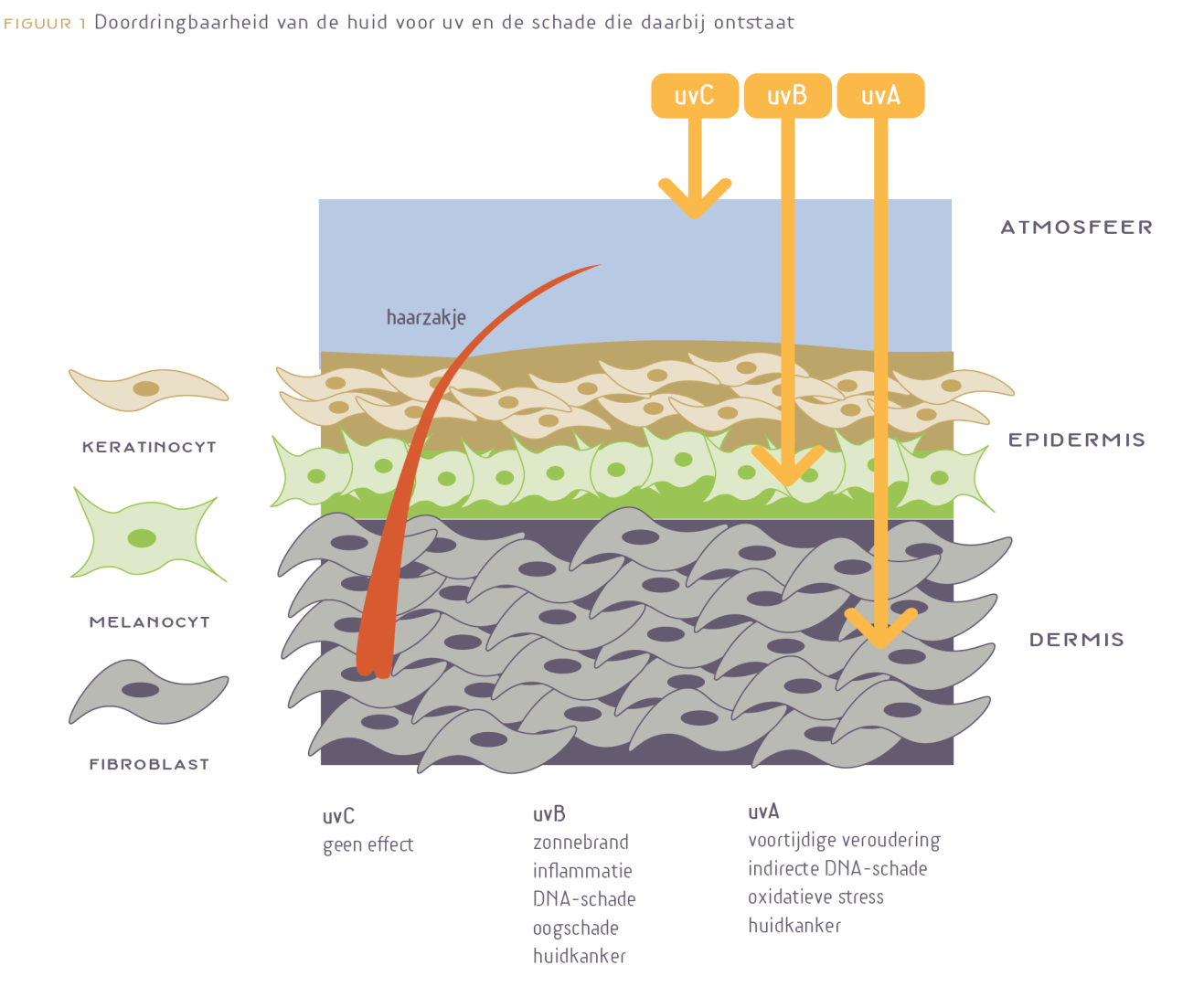
Het meeste 7DHC bevindt zich in de epidermis (‘opperhuid’); de buitenste laag van onze huid. Vooral in de stratum spinosum en stratum basale (figuur 1 en 2)4c. Dat is ook de plaats waar de meeste (eu)melanine zit. Eumelanine is een zwart biopolymeer dat zijn oorsprong vindt in het aminozuur tyrosine. Het vormt de zwarte kleur van de huid en beschermt ons door absorptie van energierijke straling en deze energievorm om te zetten in warmte. Melanine beschermt vooral tegen de schadelijke invloed van uvB en uvA (320-400 nm), maar ook de schadelijke invloed van het zichtbare licht (400-700 nm), vooral het hoogenergetische violet-blauw. Het uitermate schadelijke uvC (100-280 nm) wordt tegengehouden door de ozonlaag in de stratosfeer. UvB is de meest schadelijke straling voor de huid, maar we hebben het wel nodig voor het maken van vitamine D. Dit vraagt dus om balans. Het minder energierijke uvA dringt dieper door en wordt vooral verantwoordelijk gehouden voor de veroudering van de huid (figuur 2). Ook uvA hebben we nodig, onder andere voor de bloeddrukregulatie (zie verderop). UvA komt in tegenstelling tot uvB door glas heen en breekt vitamine D af in de huid. Te weinig vitamine D in de huid en verbranding van de huid worden beide in verband gebracht met het ontstaan van het (maligne) melanoom. Het is dus niet verstandig om achter glas te zonnen.5a-5i Uv-straling veroorzaakt naar schatting 65% van de melanomen en 90% van alle huidkanker.6
Aanpassing aan zonlicht
Lang werd aangenomen dat mensen die tijdens de evolutie vanuit Afrika naar het noorden migreerden, ‘licht van kleur werden’ zodat ze in de herfst en winter efficiënter vitamine D konden maken. Dat die lichte kleur iets met zonlicht heeft te maken, klopt nog steeds, maar de relatie met vitamine D ligt ingewikkelder. Recent genetisch onderzoek aan de stoffelijke resten van onze Europese voorouders liet zien dat de jagende en verzamelende Europeanen tot ongeveer 9.000 jaar geleden een zwarte huidskleur hadden. Dat een lichte huidskleur nodig was voor de overleving in Europa, werd hiermee dus gefalsificeerd. De lichte huidskleur (varianten van de genen SLC24A5 en SLC45A2) werd vanaf 9.000 jaar geleden geïmporteerd door Anatolische boeren die vanuit het huidige Turkije Europa binnentrokken. Van alle bekende varianten heeft een mutatie in het SLC24A5-gen (rs1426654) de sterkste invloed op de verbleking van de huid.7 Vanaf de Bronstijd, zo’n 5.000 jaar geleden, werd de immigratie van de Anatolische boeren gevolgd door de komst van een nomadisch herdersvolk, de Yamnaya, die ook een lichte huidskleur hadden (eveneens SLC24A5- en SLC45A2-varianten). Zij trokken Europa binnen vanuit Azië.2,7,44 Rond 6.000 jaar voor Christus bestond er in Europa een aanzienlijke interindividuele variatie in huidpigmentatie-niveaus.8
Het is nog onduidelijk waar de in Europa meest-voorkomende variant van het lactase-enzym, het zogenaamde -13.910*T-allel, vandaan komt. Deze variant veroorzaakt lactase-persistentie.9-9c Dat is het vermogen om ook als volwassene het melksuiker lactose in de dunne darm efficiënt te kunnen splitsen in glucose en galactose. Dit allel verscheen ongeveer 6.000 jaar geleden in Centraal Europa en verspreidde zich vervolgens razendsnel langs de routes van de Yamnaya-cultuur. Echter, de gemengde landbouw-veeteeltrevolutie was toen in Europa reeds al lang aan de gang en koemelk stond daarbij op het menu.11,11a,12 Waarschijnlijk is lactase-persistentie dan ook niet ontstaan om als volwassene ‘melk te kunnen drinken’, zoals dat in vele leerboeken en publicaties staat. Volgens de heersende hypothese zou het een selectievoordeel zijn vanwege het hoge caloriegehalte en de macro- en micronutriënten, waaronder calcium. Herders in Centraal-Azië zijn echter voornamelijk lactase-non-persistent en halen een groot deel van hun voeding uit (deels gefermenteerde) melk(producten).9a Bovendien kunnen lactase-non-persistente volwassenen per dag ten minste een enkele portie van 250 mL koemelk drinken zonder maag-darmbezwaren. En zelfs grotere hoeveelheden indien de porties verspreid worden ingenomen gedurende de dag en samen met andere voedingsmiddelen worden geconsumeerd.10 Lactose, calcium en melk zijn wel sterk met elkaar verweven, want lactose verhoogt de calciumresorptie.10a
De sterkste selectiedruk op de mens wordt veroorzaakt door zonlicht en door parasieten, schimmels, bacteriën en virussen. Klimaat en voeding oefenen minder selectiedruk uit en er bestaan veel misverstanden hieromtrent. Zo nemen de uv-straling, omgevingstemperatuur, absolute luchtvochtigheidsgraad en de neerslag af vanaf de evenaar naar het noorden en het zuiden, maar neemt in deze richtingen evenzo de biodiversiteit af en daarmee ook de selectiedruk door pathogenen.13-17 Het blijft moeilijk om in het licht van zoveel associaties de werkelijke selectiefactor aan te wijzen. Lactase-persistentie vormt waarschijnlijk een bescherming tegen de zoönosen die meegebracht werden door de dieren die tijdens de gecombineerde landbouw-veeteeltrevolutie werden gedomesticeerd. De tuberkelbacil (tuberculose) kwam naar ons toe via het rundvee en vormt maar één van de vele voorbeelden.18,19 Op het beschermende mechanisme van lactase-persistentie wordt hier niet verder ingegaan, maar het heeft te maken met het voorkómen van een levensgevaarlijke uitdroging door diarree en overgeven bij een maag-darminfectie.20 Dus een soort orale rehydratie vloeistof. Om welke reden dan ook: de lichtere huidskleur en lactase-persistentie bleken dusdanig voordelig dat deze eigenschappen in Noord-Europa nagenoeg werden gefixeerd door positieve selectie via ‘selective sweeps’.13c,14,16,21
Als een lichte huidskleur niet nodig is om de functie van vitamine D te behouden, waar is deze dan wel goed voor? Want zonder melanine is er immers een groot risico op schade door de zon. Zoals we dat, bijvoorbeeld, in extreme vorm kennen uit het ontstaan van huidkanker reeds op jonge leeftijd bij albino’s in Afrika en de epidemie van huidkanker bij witte mensen in Australië. Een lichte huid is ‘wit’, omdat deze, voor iedereen zichtbaar, de kampioen is in het reflecteren van zonlicht. Door reflectie kunnen uv-straling en zonlicht een lichte huid minder goed binnendringen. De sterkte van de reflectie van zonlicht door de huid correleert sterk met de breedtegraad en de lokale sterkte van de uv-straling.22,23 Het ziet er dus naar uit dat het onschadelijk maken van zonlicht door middel van absorptie door de melanine in een zwarte huid werd ingewisseld door de reflectie van zonlicht door een witte huid.
Reeds lang is bekend dat personen met een donkere huidskleur doorgaans een lagere vitamine D-status hebben dan personen met een lichte huidskleur, maar daarvan in hun botmetabolisme geen schadelijke gevolgen ondervinden. Integendeel: een zwarte huid gaat samen met een hogere botmineraaldichtheid en een lager risico op fragiliteitsfracturen.24 Er zijn goed gedocumenteerde raciale verschillen in de relatie tussen 25OHD, botmineraaldichtheid en het parathyreoïdhormoon (PTH). Zo is, in tegenstelling tot de Mexicaanse en witte Amerikanen, de PTH van Amerikanen met een zwarte huidskleur reeds onderdrukt bij een plasma-25OHD onder 50 nmol/L. Bij een gegeven plasma-PTH-concentratie hebben mensen met een zwarte huid een lager totaal plasma-25OHD. Hun biologisch beschikbaar gehalte aan 25OHD is echter gelijk aan dat van mensen met een witte huid.24 Dit suggereert dat mensen met een zwarte huidskleur minder vitamine D nodig hebben en mogelijk ook minder calcium om een optimale calcium-fosfaatbalans te bereiken.24,25
Genetische variatie
Hoe kan dit nu allemaal? Hiervoor moeten we niet slechts één factor, maar alle factoren begrijpen die betrokken zijn bij de interactie tussen het 1,25OHD-hormoon2,7 en de vitamine D-receptor. Tevens dienen daarbij alle andere, niet-vitamine D-gerelateerde, functies van onze huid te worden betrokken, want diverse daarvan zijn eveneens afhankelijk van het zonlicht (zie verderop). Slechts als we al deze functies simultaan beschouwen, kunnen we begrijpen hoe Europeanen en Aziaten zich hebben aangepast aan de veranderende communicatie tussen hun huid en de zon, toen hun voorouders vanuit Afrika naar het noorden trokken.
Met betrekking tot de uiteindelijke werkzaamheid van vitamine D op zijn receptor zijn onder andere belangrijk: de hoeveelheid 7DHC in de huid, de efficiëntie van het vitamine D-transport in het bloed, vitamine D-opslagvormen, de efficiëntie van de omzetting van vitamine D naar 1,25OHD en de afbraak daarvan, alsmede de gevoeligheid van de vitamine D-receptor voor het vitamine D-hormoon. Elk van deze factoren blijkt tijdens de out-of-Africa-migratie naar hogere breedtegraden onderhevig te zijn geweest aan aanpassing door middel van mutatie-selectie (Darwin/Mendel). Er bestaan veel varianten, om niet te spreken over de vele combinaties die daarvan mogelijk zijn. Deze kunnen onder andere veroorzaken dat een persoon met een lagere vitamine D-status, dat wil in huidige terminologie zeggen een laag plasma-25OHD, toch een prima werking kan hebben van het vitamine D-hormoon. Vitamine D-functie, dus fenotype, is het enige dat belangrijk is. De evolutie stuurt op fenotype: genotype staat in dienst van fenotype, niet andersom. Zo werd onder andere gevonden dat de huidige Europeanen meer 7DHC in hun huid hebben dan Afrikanen en Aziaten, en ze dus bij een lagere uvB-straling toch evenveel vitamine D in de huid kunnen aanmaken. De hiervoor benodigde mutaties in het enzym 7-dehydrocholesterol-reductase (rs12785878 en rs7940244) zijn bekend. Dit enzym zet 7DHC om in cholesterol.2,7 In lijn met een lagere 7-dehydrocholesterol-reductase-activiteit hebben mensen met een aangeboren stofwisselingsziekte waarbij dit enzym niet, of sterk verminderd, werkzaam is (het ‘Smith–Lemli–Opitz-syndroom’) een verlaagde cholesterolsynthese met een verhoogd plasma-7DHC en plasma-25(OH)D, zonder vitamine D-toxiciteit.25b
Reeds lang kennen we ook de varianten in het vitamine D-bindend eiwit (VDBP)24,25. VDBP gaat door als de ‘transporteur’ van vitamine D en zijn metabolieten door het bloed. Er bestaat een positieve relatie tussen het plasmagehalte van dit VDBP en het plasma-25OHD. VDBP gaat een relatief zwakke binding aan met vitamine D en een sterkere met zijn metabolieten 25OHD en 1,25OHD. De binding met 25OHD is het sterkst. VDBP is een polymorf eiwit:25a er zijn meer dan 120 genetische varianten van bekend. Drie daarvan komen relatief veel voor, geheten: Gc1s, Gc1f en Gc2. Gc verwijst naar het gen en staat voor group-specific component. Afrikanen hebben vooral de Gc1f-variant en deze veroorzaakt een lager plasma-VDBP, en dus ook een lager 25OHD, vergeleken met de Gc1s-variant, die vooral bij Europeanen voorkomt. Genotype Gc2 komt ook meer voor bij witte mensen.25a,26 Deze drie varianten bepalen in sterke mate het VDBP-gehalte in het bloed in de volgorde Gc1s > Gc2 > Gc1f.24,26 Ook is na het toedienen van een hoge dosis vitamine D aan personen met een lage vitamine D-status de stijging van het plasma-25OHD sterker in de volgorde Gc1s > Gc2 > Gc1f.27 Er zijn ook verschillen in de bindingssterkte met vitamine D en metabolieten.24
Ondanks de lagere VDBP en 25OHD-gehaltes die samen gaan met een zwarte huid, is het gehalte aan beschikbaar 25OHD voor mensen met een zwarte huid en een witte huid gelijk.24 Hogere VDBP-gehaltes correleren niet alleen met een lagere kans op vitamine D-deficiëntie, maar bijvoorbeeld ook met een verlaagd risico op multiple sclerose en reumatoïde artritis. Ook zijn de VDBP-fenotypen gelinkt aan de gevoeligheid voor, of resistentie tegen, osteoporose, ziekte van Graves, Hashimoto’s thryreoïditis, diabetes, COPD, aids en sarcoïdose.28,29 Of elk van deze aandoeningen met vitamine D te maken heeft, is onzeker, want naast de binding van vitamine D en vitamine D-metabolieten, heeft VDBP ook vele andere functies, waaronder het binden van vetzuren, endotoxine-transport, neutrofiel-chemotaxis, T-celrespons, de klaring van actine uit het bloed en de invloed van VDBP-macrofaag-activerende factor op het botmetabolisme en kanker.30,31a
Zoals verwacht leidt een homozygote deletie van het Gc-gen tot onmeetbaar-lage gehaltes aan VDBP en 25OHD, en lage gehaltes van het 1,25OHD-hormoon. Toch vertoonde de aangedane persoon, maar ook muizen die geen VDBP maken, nagenoeg geen tekenen van botziekte, wat suggereert dat VDBP niet nodig is voor het vitamine D-transport.25,31 De huidige gedachte is dat hogere VDBP-gehaltes, zoals die dus vooral worden gezien bij Europeanen, fungeren als een circulerend, snel mobiliseerbaar, reservoir van 25OHD. Bij het uitblijven van de synthese van vitamine D, zoals in de winter, verschaft deze opslagvorm bescherming tegen het ontstaan van vitamine D-deficiëntie.26 Deze snel beschikbare voorraad bestaat dus naast een schijnbaar langere-termijnvoorraad van 25OHD, die in de spieren ligt opgeslagen in de vorm van een VDBP-actine-complex en een voorraad van vitamine D die in het vetweefsel aanwezig is (zie ook verderop).32
De nieuwe kijk op de functie van het VDBP, maar ook de zwakkere binding van vitamine D en metabolieten aan albumine, indien vergeleken met de binding aan VDBP, benadrukt het belang van hun vrije vormen in de circulatie, wat bekend staat als de ‘vrije-vitamine D-hypothese’. Hierin wordt het vrij in het plasma opgeloste vitamine D gezien als de belangrijkste vorm waarin vitamine D (hier wordt dus niet bedoeld zijn metabolieten) wordt opgenomen in de meeste extra-renale weefsels, terwijl, zoals voor ieder hormoon, dus ook voor het 1,25OHD-hormoon, geldt dat het de vrije (dus de niet-eiwitgebonden) vorm is, die voor zijn functie een interactie aangaat met zijn receptor.26,33-37 Los van de opname van het vrije vitamine D bestaat een opnamesysteem voor het VDBP met de daaraan gebonden vitamine D en metabolieten (dus vooral 25OHD). Dit wordt verzorgd door het megaline-cubiline-receptorcomplex, dat vooral operationeel is in de niertubuli en de spieren, maar ook in vele andere weefsels waaronder de darmen, placenta en dooierzak.25a,30,31a,32,37a,b Het megaline-cubiline-receptorcomplex in de niertubuli is onder andere verantwoordelijk voor de terugresorptie van het gefiltreerde VDBP, met het daaraan gebonden 25OHD, uit de primaire urine, waarna 25OHD in deze cellen wordt omgezet in het vitamine D-hormoon en vervolgens in de circulatie wordt uitgescheiden voor zijn endocriene functie. Dit is de reden van de reeds lang bekende sterke relatie tussen de filtratiefunctie van de nier en de circulerende gehaltes aan het vitamine D-hormoon en dus ook de daling van de vitamine D-hormoongehaltes (en de stijging van de PTH en FGF23) bij een gecompromitteerde filtratiefunctie.32 De opname van VDBP, met het daaraan gebonden 25OHD, in de spieren leidt tot een lokale 25(OH)D-voorraad, die kan worden gemobiliseerd bij spierbeweging. Het in het vetweefsel opgeslagen vitamine D wordt gemobiliseerd bij vasten, waarbij moet worden gedacht aan de voedselschaarste die onze voorouders ondergingen gedurende de winter.25,32,33,37a-c
Naast variatie in de gehaltes aan 7DHC in de epidermis en het transport/opslag via VDBP zijn eveneens varianten gevonden in CYP2R1 (de belangrijkste 25-hydroxylase van vitamine D) en CYP24A1 (die zorg draagt voor de de-activering van 25OHD en 1,25OHD). De halfwaardetijd van 25OHD wordt ook nog eens beïnvloed door de calciuminname.32 Iedere stap in de syntheseroute van vitamine D naar 1,25OHD, maar ook de de-activering van de producten door CYP24A1, wordt beïnvloed door magnesium.38-40 Deze factoren worden hier niet verder besproken.
Het is duidelijk dat verandering van huidskleur maar één van de vele mogelijkheden was voor de aanpassing aan de lagere uvB-stralingsintensiteit op hogere breedtegraden. De talrijke genetische varianten, en de snelheid waarmee ze zich in de Europese bevolking hebben verspreid, getuigen van het belang om de functies van vitamine D tijdens de evolutie intact te houden. Welke van de vele vitamine D-functies daarbij het meest kritisch was, en mogelijk nog steeds is, is onbekend. Het is ook mogelijk dat aanpassing door sommige populaties, zoals in Centraal-Azië, niet is opgetreden vanwege mutatie-selectie (nature) of de epigenetica (nature/nurture) maar via veranderde cultuur (nurture), zoals het fermenteren van melk en daardoor een hogere calciuminname.9a De focus van voedingscommissies op de loutere functie van vitamine D in het botmetabolisme, omdat daar toevallig het meeste onderzoek aan is gedaan, vormt dan ook een onderschatting van de talrijke mechanismen waarmee de zon vanaf de oorsprong van het leven op aarde met levende organismen communiceert. Het vragen naar bewijs via een gerandomiseerd onderzoek zegt vooral iets over de weinig doordachte manier waarop we tegenwoordig in de volksgezondheid en gezondheidszorg denken te moeten redeneren.
De functies van huidskleur
Door het verlies van melanine en de verhoging van het gehalte aan 7DHC in de epidermis werd het gemakkelijker om vitamine D te maken in de witte huid, maar daardoor nam de kans op schade toe. Zo kan bij gelijke expositie aan zonlicht worden aangetoond dat de vorming van ‘cyclobutaan-pyrimidine-dimeren’ (CPD) in het DNA sterker is in de volgorde Kaukasische huid > Aziatische huid > zwarte huid.41 Het gaat hier om één van de vele verbindingen die in het DNA kunnen ontstaan bij blootstelling aan zonlicht. Als dergelijke DNA-schade niet wordt gerepareerd, kan dit tot mutaties leiden. Uit epidemiologisch onderzoek is reeds lang bekend dat de witte huid veel meer kans heeft op het ontwikkelen van de vormen van huidkanker die door de zon worden veroorzaakt.41
Inzake de slechtere bescherming door melanine en de vaak in de literatuur benadrukte ‘betere vitamine D-synthese in de witte huid’ is het belangrijk om te weten dat melanine vooral gelokaliseerd is in het deel van de opperhuid (de stratum basale van de epidermis) die grenst aan de daaronder gelegen lederhuid (de dermis, figuur 2)41. In deze stratum basale bevinden zich de melanocyten, die melanine maken en het als ‘pakketjes’ in de vorm van melanosomen overdragen aan de direct-omringende keratinocyten. Deze verwerken de melanosomen en deponeren de melanine vervolgens rondom hun celkernen om het daarin gelegen kwetsbare DNA tegen de straling van de zon te beschermen (figuur 2).42,43 Die bescherming is vooral nodig tegen uvB dat directe DNA-schade kan veroorzaken en daarmee bijdraagt aan het ontstaan van huidkanker. Maar ook tegen uvA dat vooral in verband wordt gebracht met de veroudering van de huid.42 Het is duidelijk dat, door de lokalisatie van de vitamine D-precursor 7DHC vooral boven de melaninelaag, melanine geen volledig onderdrukkende invloed kan hebben op de synthese van vitamine D en nog wel het minst in een witte huid.2,7
Wat moet melanine naast ons DNA nog meer beschermen? In de dermis bevinden zich de bloedvaten, lymfevaten, zenuwen, talgkliertjes, zweetkliertjes en haarzakjes (figuur 1)5. Deze zijn uitermate kwetsbaar voor het oplopen van schade door zonlicht. Schade aan de zweetkliertjes ontregelt de thermoregulatie. Het boven de dermis, dus in de epidermis, gelokaliseerde melanine absorbeert het zonlicht voordat de daaronder gelegen gevoelige structuren worden bereikt. Het maakt daarmee vooral uv-straling onschadelijk, maar ook het daaraan grenzende zichtbare blauwe en groene licht. Dat blauw-groene deel van het zichtbare spectrum (HEVIS, high-energy visible light) is vanwege zijn hoge energie eveneens schadelijk maar dringt minder diep door in de huid dan bijvoorbeeld rood licht. Eigenlijk is alle straling schadelijk, dus gaat het weer eens over balans. Het doordringend vermogen gaat in de volgorde infrarood > rood > geel > groen > blauw > uvA > uvB. Hoe lager de energie van de straling, hoe verder deze doordringt en ook hoe lager het absorberend vermogen van deze straling door melanine. De potentieel-schadelijke invloed van het zichtbare deel van zonlicht wordt mogelijk te veel onderschat.
Eén van de stoffen die door melanine moet worden beschermd, is folaat (vitamine B9/B11). Dit (oranje-gele) wateroplosbare vitamine stroomt constant door onze bloedvaten en is erg gevoelig voor fotochemische afbraak door zonlicht, vooral door uvA en uvB. Folaatdeficiëntie is een evident evolutionair nadeel, omdat het neuralebuisdefecten, en daardoor kindersterfte, kan veroorzaken. De witte huid bevat nagenoeg geen (eu)melanine maar beschermt, zoals gezegd, vooral door reflectie: vandaar die witte kleur. Een witte huid bevat echter evenveel melanocyten41 en verkrijgt extra bescherming door deze cellen melanine te laten aanmaken na een sterke blootstelling aan zonlicht, zoals in de zomer.44 Dit wordt ‘facultatieve’ pigmentatie genoemd, i.t.t de ‘constitutieve’ in een zwarte huid.41 Melanogenese in een witte huid moet worden gezien als een reactie op ‘gevaar’ (zonlicht is een danger-associated molecular pattern, afgekort: DAMP) en werkt klassiek via het p53-systeem (de ‘beschermengel van ons DNA’). Ook kan de epidermis dikker worden.41 Reflectie van zonlicht door een witte huid is vooral prominent rondom een golflengte van 545 nm (groen) en dat is niet toevallig de golflengte die door het rode oxyhemoglobine (HbO2) wordt geabsorbeerd. HbO2 absorbeert het (complementaire) groene licht en daardoor is het gereflecteerde licht rood. Lichtabsorptie door oxyhemoglobine is in het reflectiespectrum te zien als het karakteristieke W-absorptiemotief bij golflengtes van 540 en 576 nm. Deze is intensiever te zien als, om wat voor reden dan ook, de huiddoorbloeding van vooral een witte huid toeneemt (erythema).
Dat een witte huidskleur met een hogere vitamine D-synthese heeft te maken, kan mogelijk ook worden ontleend aan de waarneming dat in alle bevolkingen de vrouwen een lichtere huidskleur hebben dan de mannen. Waarschijnlijk is dit bedoeld om meer vitamine D te kunnen aanmaken tijdens de zwangerschap. Dat dit ook bedoeld is voor de lactatie, zoals in de literatuur kan worden gelezen,23 is onwaarschijnlijk, want moedermelk bevat onvoldoende vitamine D om aan de behoefte van de pasgeborene te kunnen voldoen. Ook niet na langdurige toediening van een hoog gedoseerd vitamine D-supplement aan de moeder. Het kind dient vóór de geboorte een vitamine D-voorraad op te bouwen, dus het gaat hierbij vooral om transplacentatransport.44a
Huidskleur lijkt dus onderdeel te zijn van een compromis waarbij de functies van vitamine D intact werden gehouden en de schadelijke effecten van de zon werden geminimaliseerd via modulatie van de dikte van de epidermis en reflectie (lichte huidskleur) en absorptie (melanine, urocaanzuur) van straling.41,45 Met het verschijnen van de witte huid lijkt een nieuwe strategie te zijn ontwikkeld, waarbij meer zonlicht wordt gereflecteerd, compensatie is opgetreden voor de nu verlaagde uvB-expositie van de epidermis (en de daarmee samenhangende vitamine D-synthese) door aldaar meer 7DHC aan te maken, en overschakeling van de constitutieve eumelanine-synthese van de zwarte huid naar de facultatieve eumelanine-synthese van de witte huid, teneinde de onder de epidermis gelegen structuren te beschermen op het moment dat het nodig is (zomer). In werkelijkheid gaat het echter om nog meer (hier niet besproken) lokale en systemische factoren die afhankelijk zijn van de manier waarop de zon met onze huid communiceert.42,46,46a Deze zijn onder andere belangrijk voor de bloeddrukregulatie (synthese van stikstofmonoxide uit nitraat o.i.v. uvA)47-49, het dag-nachtritme (synthese van 6-formylindolo[3,2-b]carbazole, afgekort FICZ, uit tryptofaan)50-53, immuunsuppressie, barrièrefunctie en uv-absorptie via de synthese van urocaanzuur uit histidine in het stratum corneum,54,55 en onze stemming (synthese van neuropeptiden).56,57
Samenvatting, consequenties en conclusies
De grootste evolutionaire druk die de mens ervaart, wordt gevormd door het zonlicht en pathogenen.13-17 Het samenvoegen van gegevens uit de archeologie en de genetica heeft ons eraan herinnerd dat er meerdere combinaties van mutaties kunnen worden benut om ons via mutatie-selectie (Darwin/Mendel) aan te passen aan het weinige zonlicht op hogere breedtegraden. Verandering van huidskleur blijkt slechts één van de vele mogelijkheden en ging gepaard met aanpassingen van de hoeveelheid 7DHC in de huid, de efficiëntie van vitamine D-transport/opslag in het bloed, de efficiëntie van de omzetting van vitamine D naar het functionele 1,25OHD-hormoon en de de-activering daarvan, en ook de gevoeligheid van de vitamine D-receptor voor 1,25OHD.2,7 Dit zijn slechts de aanpassingen die nodig waren voor het behoud van de functies van vitamine D. Hoe dit uitpakte voor de vele andere functies van onze huid staat nog in de kinderschoenen.
Eén consequentie van de nieuwe inzichten is dat de huidige bepaling van de vitamine D-status, via de analyse van het totaal plasma-25OHD ons niet de meest nauwkeurige informatie verschaft over een optimale werking van vitamine D. Want de interpretatie van de uitslag is op complexe wijze afhankelijk van de genetica van de betreffende persoon (nature) en mogelijk de cultuur van de voorouders (nurture, denk aan fermentatie). Het roept ons op om naar een betere parameter voor de vitamine D-status uit te kijken. Zo kan een optimale PTH mogelijk dienen als een alles-overkoepelde functionele parameter voor het bepalen van een goede werking van vitamine D in de calcium-fosfaathomeostase. De PTH heeft echter ook beperkingen want deze is eveneens afhankelijk van de genetica en omgevingsfactoren, waaronder roken, BMI, bewegen en uiteraard de nutriënten vitamine D en calcium. Roken, vitamine D en calcium verlagen de PTH, terwijl een hogere BMI en meer bewegen de PTH verhogen.58
Tot nader orde lijkt het streven naar een plasma-25OHD van ten minste 75 nmol/L (of ‘80 is prachtig’) voor iedereen een praktische aanbeveling, die volgens de werkelijke vitamine D-experts1 is gebaseerd op ‘het tot nu toe beste bewijs’ en zoals dat ook door de bedenker van evidence-based medicine (Dr. David Sackett) oorspronkelijk was bedoeld.59 Het heeft weinig zin te wachten op een gerandomiseerde interventiestudie met harde eindpunten en een looptijd van 30 jaar, die dus niemand gaat doen. Traditioneel levende Maasai en Hadzabe in Tanzania hebben een plasma-25OHD rond de 115 nmol/L (range: 71-158 nmol/L) en voor zwangere Maasai is dit 148 mol/L (65-218 nmol/L). Echter, indien deze waarden als targets worden gezien voor de huidige ‘westerse’ cultuur, moet men ‒ naast het verschil in genetica ‒ de gehele leefstijl en voeding van deze traditioneel levende populaties beschouwen, waaronder beweging, vasten-voedingscyclus, BMI en de innames van vitamine K2, magnesium en calcium.60
Slechts door de, tijdens de evolutie ervaren, selectiedruk van een veranderende omgeving te begrijpen, kunnen we snappen wie we zijn, voor welke omgeving we zijn bedoeld (Darwin) en hoe we een optimale gezondheid kunnen bereiken.61
Dankwoord
Ik dank em. prof. dr. ir. Gertjan Schaafsma (Scherpenzeel), drs. Tondo (A) van Rijssen, (dermatoloog Stadkanaal en Emmen) en Peter Borsboom (Den Haag) voor hun kritisch commentaar op, respectievelijk, de voedingsgerelateerde, dermatologische en natuurkundige (optica) onderdelen.